Rohstoffanalyse in der Getreidewirtschaft
Schnellmethoden zur Mykotoxinbestimmung
Rohstoffanalyse in der Getreidewirtschaft
Schnellmethoden zur Mykotoxinbestimmung

Rohstoffanalyse in der Getreidewirtschaft
Schnellmethoden zur Mykotoxinbestimmung
Verschärfte Grenzwerte, steigende klimatische Risiken und häufige Ko-Kontaminationen erhöhen den Bedarf an schnellen, zuverlässigen Analysen. Multiplex-Immunoassays erfassen mehrere Mykotoxine gleichzeitig, reduzieren den analytischen Aufwand und ermöglichen fundierte Entscheidungen entlang der gesamten Prozesskette.
Mykotoxine zählen zu den wichtigsten lebensmittelrelevanten Kontaminanten in der Getreidewirtschaft. Sie entstehen als Stoffwechselprodukte verschiedener Pilze und können bereits in geringen Konzentrationen gesundheitsschädlich sein. Je nach Toxin reichen die Wirkungen von immunsuppressiven und östrogenen Effekten über Nieren- und Leberschäden bis hin zu karzinogenen Eigenschaften.
Besonders relevant sind Toxine der Pilzgattungen Aspergillus, Fusarium, Penicillium und Trichoderma. Zu den regulatorisch wichtigsten Verbindungen gehören Deoxynivalenol (DON), Zearalenon (ZEN), Ochratoxin A (OTA), T-2- und HT-2-Toxin, Aflatoxine (AFL) sowie Fumonisine (FUM).
Die Bedeutung einer zuverlässigen Analytik nimmt kontinuierlich zu. Einerseits werden regulatorische Grenzwerte innerhalb der EU stetig erweitert und verschärft. Ein aktuelles Beispiel ist die Einführung von Höchstgehalten für die Summe aus T-2- und HT-2-Toxin in Lebensmitteln seit Juli 2024. Außerdem wurden niedrigere Höchstgehalte für Ergot-Sklerotien (Mutterkorn) und Ergotalkaloide beschlossen. Deren Anwendungszeitpunkte wurden allerdings für einzelne Produktgruppen um ein bzw. vier Jahre verschoben, da die praktische Umsetzbarkeit noch nicht vollständig gewährleistet ist. Andererseits erhöhen klimatische Veränderungen das Kontaminationsrisiko. Extremwetterereignisse und steigende Temperaturen begünstigen Pilzwachstum und Toxinbildung. Mutterkorn befällt normalerweise hauptsächlich Roggen. Tritt jedoch bei Weizen aufgrund ungünstiger Wetterbedingungen eine Sekundärblüte auf, kann auch dort ein verstärkter Mutterkornbefall auftreten, wie der Sommer 2025 gezeigt hat.
Da Mehrfachkontaminationen in Getreide die Regel sind, steigt der Bedarf an Verfahren, die mehrere Mykotoxine parallel erfassen können. Studien berichten Ko-Kontaminationen in rund 55% der untersuchten Proben. Besonders häufig sind Kombinationen wie DON + ZEN in Weizen oder DON + FUM in Mais (Streit et al. 2013, World Mycotoxin Journal). Schnelle Screeningmethoden spielen daher eine zentrale Rolle, um Risiken frühzeitig zu erkennen und fundierte Entscheidungen zur Annahme und Freigabe von Rohwaren zu treffen.
Zur Bestimmung von Mykotoxinen stehen unterschiedliche analytische Methoden zur Verfügung, die sich hinsichtlich Genauigkeit, Geschwindigkeit und Aufwand deutlich unterscheiden.
Als Goldstandard gilt die LC-MS/MS (Liquid Chromatography Tandem Mass Spectrometry). Die Methode ermöglicht eine hochselektive Quantifizierung zahlreicher Mykotoxine in einem Analyselauf. Die Probenvorbereitung umfasst Extraktion, ggf. Aufreinigung (z. B. per Immunoaffinitätssäule), chromatographische Trennung sowie massenspektrometrische Detektion mit isotopenmarkierten internen Standards. Dank ihrer hohen analytischen Sicherheit ist die LC‑MS/MS die bevorzugte Methode für Bestätigungsanalysen und regulatorische Fragestellungen. Allerdings ist sie mit hohen Gerätekosten, qualifiziertem Personalbedarf und Analysezeiten von zwei bis sechs Stunden verbunden. Bei einer Durchführung über ein Handelslabor liegt das Ergebnis erst nach mehreren Tagen vor. Lateral-Flow-Tests und ELISA zählen zu den etablierten Immunoassay-Schnellmethoden. Das Grundprinzip dieser Immuoassay ist, dass ein Mykotoxin aus der Probe mit einem markierten bzw. immobilisiertes Toxin-Analog um die Bindungsstellen der Antikörper konkurriert. Je mehr Toxin in der Probe vorhanden ist, desto weniger markiertes Molekül kann gebunden werden. Das gemessene Signal ist daher invers proportional zur Toxinkonzentration.
Beim Lateral-Flow-Test findet diese Reaktion auf einem Teststreifen statt: Die Probe wandert durch Kapillarkräfte über verschiedene Reaktionszonen und die Bindung wird meist als farbige Linie sichtbar oder mit einem Reader gemessen. Sie liefern Ergebnisse innerhalb weniger Minuten und benötigen nur minimale Laborausstattung. Allerdings sind sie meist nur semiquantitativ und zudem stark abhängig von Matrixeffekten und Probenvorbereitung. Beim ELISA erfolgt die Immunreaktion dagegen in einer Mikrotiterplatte mit immobilisierten Toxin-Analog auf der Plattenoberfläche. Nach mehreren Inkubations- und Waschschritten wird eine enzymatische Farbreaktion ausgelöst, deren Intensität photometrisch gemessen wird und eine quantitative Messung der Toxinkonzentration ermöglicht. ELISA-Tests sind in vielen Qualitätssicherungslaboren etabliert. Aufgrund der Inkubationsphasen und Waschschritte beträgt die Analysedauer typischerweise zwei bis vier Stunden. Ein weiterer Nachteil beider Verfahren ist, dass nur ein einzelner Parameter pro Test bestimmt werden kann. Um effizient auf Ko-Kontaminationen zu testen, müssen entsprechend viele Tests parallel durchgeführt werden. Außerdem sind diese Tests stark martrixabhängig und müssen für jede einzelne Matrix neu validiert werden.
Eine neuere Entwicklung stellt der Suspension Array Fluorescence Immuno Assay (SAFIA) dar. Dieses Verfahren kombiniert Eigenschaften klassischer Immunoassays mit moderner Multiplex-Technologie.
Statt auf einem Teststreifen oder der Plattenoberfläche basiert das Prinzip auf unterschiedlich farblich kodierten Partikeln, die jeweils mit einem spezifischen Toxin-Analog beladen sind. Da jeder Farbcode eindeutig einem Mykotoxin zugeordnet ist, können mehrere Analyten in einem einzigen Messlauf bestimmt werden. Nach Mischen der Partikel mit Probe und Primärantikörpern konkurrieren freie Mykotoxine aus der Probe mit den partikelgebundenen Toxin-Analoga um die Antikörperbindung. Anschließend bindet ein fluoreszenzmarkierter Sekundärantikörper und die Partikel werden mittels Durchflusszytometrie ausgelesen: Jeder Partikel fließt einzeln durch einen Laserstrahl, wobei Farbcode und Fluoreszenzintensität gleichzeitig erfasst werden und so die Konzentration mehrerer Toxine in einer Messung bestimmt werden kann. Durch die gezielte Messung der Partikel und die spezielle Partikeloberfläche spielen Matrixeffekte eine untergeordnete Rolle.
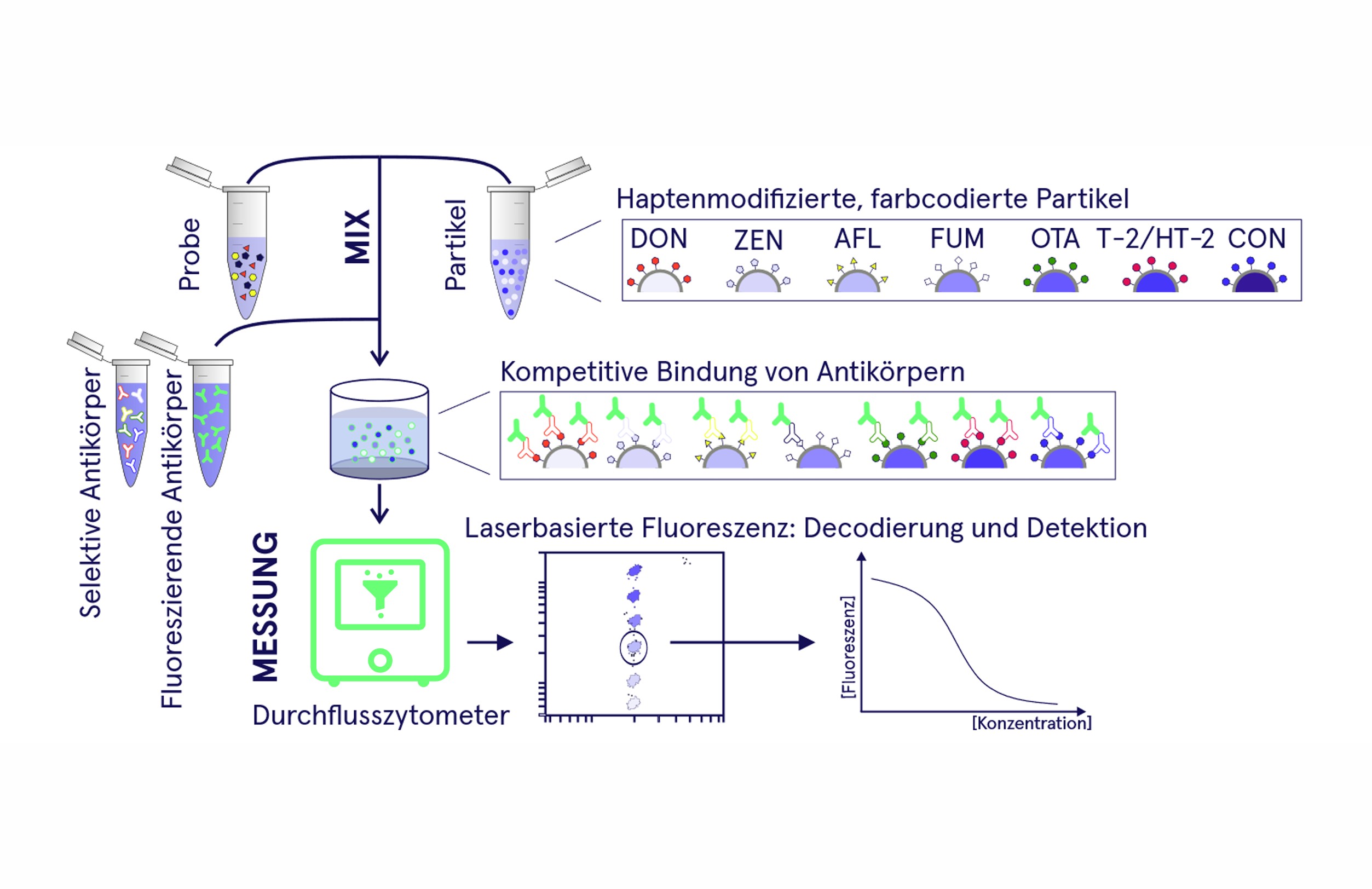
Mit der patentierten Technologie lassen sich also dank Multiplexing Ko-Kontaminationen effizient erfassen und das ohne Probleme durch Matrixeffekte.
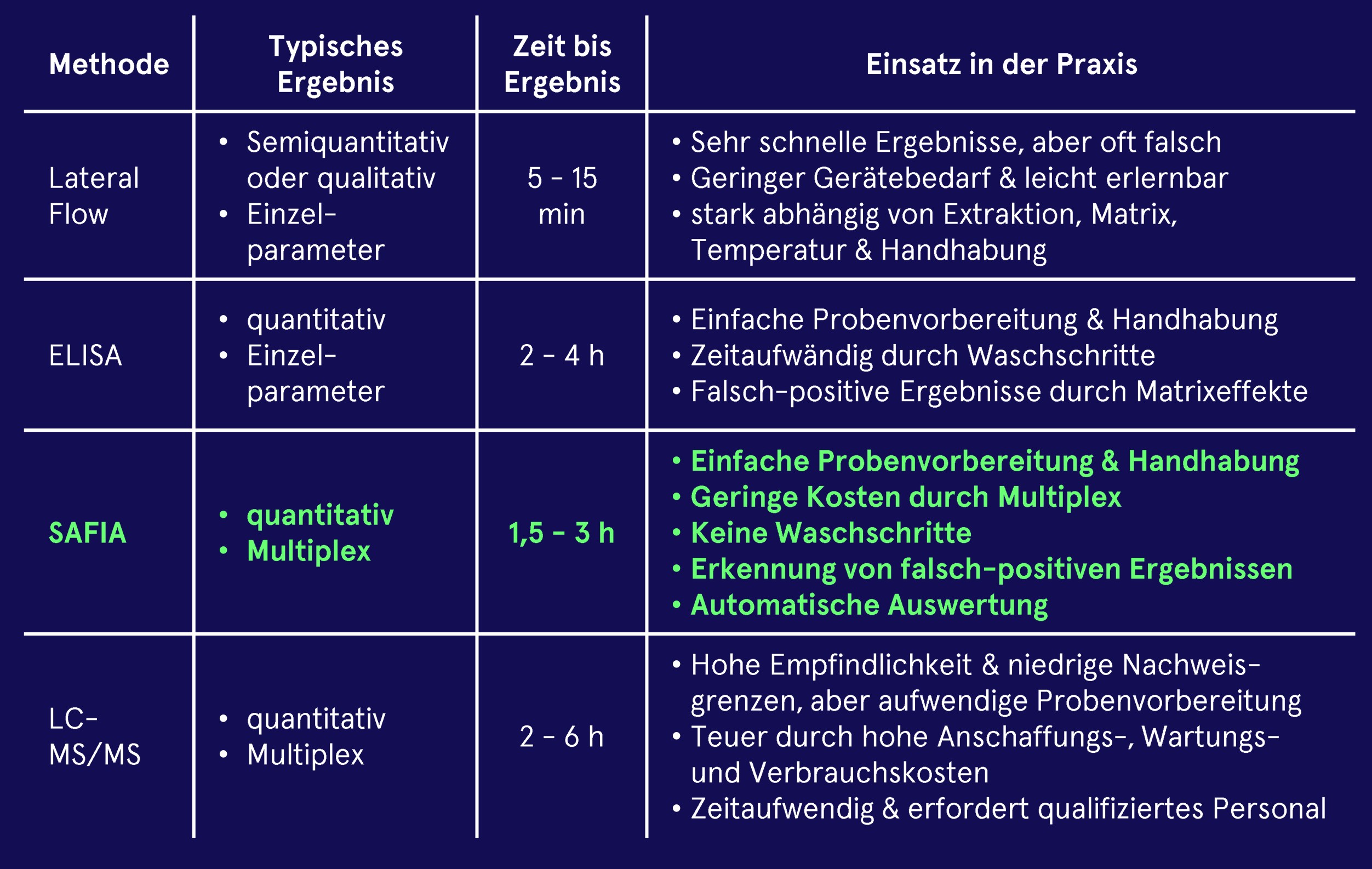
Das Unternehmen SAFIA Technologies aus Berlin arbeitet derzeit intensiv an der Weiterentwicklung seiner Schnellmethoden, um zusätzliche regulatorisch relevante Mykotoxine wie Ergotalkaloide, Alternaria-Toxine und Patulin in die Analytik einzubeziehen.
Der Bedarf an schnellen, zuverlässigen Analysen steigt. Während LC-MS/MS der Goldstandard für Bestätigungsanalysen bleibt, gewinnen die Multiplex-Immunoassays als Screeningwerkzeug zunehmend an Bedeutung. Sie ermöglichen fundierte Entscheidungen entlang der gesamten Prozesskette und leisten damit einen wichtigen Beitrag zur Lebensmittelsicherheit und wirtschaftlichen Stabilität der Getreidewirtschaft.
Autorin: Svenja Elsner, Technical Solutions Manager bei der SAFIA Technologies GmbH
Bereits Abonnent der M+M Print oder Print plus Online ?
Als Abonnent der Mühle + Mischfutter erhalten Sie diesen Zugriff gratis.
Mühle + Mischfutter Online Abo inklusive M+ Online
Unbegrenzter Zugang zu allen M+ Inhalten
Regelmäßiger Newsletter
Bequemer digitaler Zugang
Unterstützung unabhängiger Fachberichterstattung
Meldungen zu diesem Artikel
Weiterlesen
Unsere Experten zu diesem Thema
Personen aus diesem Artikel
Firmen aus dem Artikel
SAFIA Technologies entwickelt seit 2020 analytische Lösungen für eine zuverlässige und praxisnahe Lebensmittelsicherheitsprüfung. Das Unternehmen verbindet wissenschaftliche Expertise mit anwendungsorientierter Technologie, um Analysen effizienter und präziser zu gestalten. Im Mittelpunkt stehen Verfahren, die sich für den praktischen Einsatz eignen und zu einer belastbaren Qualitätskontrolle beitragen.




.jpeg)


.jpeg)


.jpeg)
.jpeg)